- اثرات شگفتانگیز نفس عمیق!
- هشدار درباره عوارض ماسک زدن زیاد
- تأثیر ماسک زدن بر میزان اکسیژن دریافتی
- استفاده از نمک دریایی به جای نمک شیمیایی
- علت تمایل ما به بستنی، شکلات، چیپس چیست؟
- ۷درس زندگی ازرویا نونهالی
- دوستت دارم به زبانهای مختلف
- بزرگان درباره راهپیمایی اربعین چه گفتند؟
- آیا مساله مهدویت و ظهور منجی در تمام ادیان الهی وجود دارد؟
- منابع اهل سنت در مورد وجود مقدس امام زمان علیه السلام كدامند؟
آخرین مطالب
امکانات وب
بنزوات سدی
بنزوات سدیم(E۲۱۱) دارای فرمول شیمیایی NaC۶H۵CO۲است. این ماده نمک اسید بنزوئیک است و به همین شکل محلول در آب است. می توان آن را از ترکیب هیدروکسید سدیم و اسید بنزوئیک تولید کرد.
| |
مصارف
سدیم بنزوات یک ماده ی نگهدارنده ی غذایی است و در محیط اسیدی از فعالیت باکتری ها و قارچ ها جلوگیری می کند. این ماده بیش از همه در غذاهای اسیدی مثل چاشنی های سالاد (سرکه)، نوشابه های گازدار (اسید کربنیک)، مرباها و آبمیوه ها (اسید سیتریک)، ترشی جات (سرکه)، و سس ها استفاده می شود. همچنین در مواد دیگر مانند برخی داروها و شامپوها نیز به کار می رود. سدیم بنزوات را بر روی محصول با همین نام یا E۲۱۱ مشخص می کنند.
این ماده همچنین در مواد آتش بازی به عنوان سوخت ترقه های موشکی به کار می رود زیرا به سرعت می سوزد و صدای سوت تولید می کند.
بنزوات سدیم از خنثی سازی اسید بنزوئیک توسط هیدروکسید سدیم حاصل می شود.[۱]اسید بنزوئیک به مقادیر کم در آلو، گوجه، دارچین، میخک، و سیب یافت می شود. با این که اسید بنزوئیک نگهدارنده ی مؤثرتری است اما معمولاً از بنزوات سدیم به عنوان نگهدارنده غذایی استفاده می شود زیرا اسید بنزوئیک به خوبی در آب حل نمی شود.[۱]غلظت مجاز به عنوان نگهدارنده غذایی توسط FDA به ۰٫۱۱٪ وزنی محدود شده است. برنامه ی بین المللی ایمنی شیمیایی برای دزهای ۶۴۷-۸۲۵mg/kg وزن بدن در روز تأثیر منفی ای شناسایی نکرد.[۲][۳]
گربه ها تحمل خیلی کمتری در مقابل اسید بنزوئیک و نمک های آن نسبت به موش ها دارند.[۴]با این حال بنزوات سدیم به عنوان افزودنی در غذای حیوانات تا مقادیر ۰٫۱٪ توسطAFCOمجاز اعلام شده است.[۵]
مکانیسم نگهدارندگی غذا
این مکانیسم با جذب اسید بنزوئیک توسط سلول آغاز می شود. اگر PH سلول به مقادیر ۵ یا کمتر کاهش یابد فرآیند تخمیر گلوکز توسط فسفوفروکتوکیناس تا ۹۵٪ کاهش می یابد.[۶]
سلامتی و ایمنی
بنزوات سدیم و بنزوات پتاسیم در ترکیب با اسید آسکوربیک (ویتامین ث، E۳۰۰) تولید بنزن می کنند، که یک سرطان زای شناخته شده است. با این حال، مقادیر آن کمتر از میزانی است که خطرناک شناخته می شود.[۷]حرارت، نور و زمان نگهداری می توانند بر نرخ تولید بنزن تأثیرگذار باشند.
پروفسور پیتر پایپر در دانشگاه شفیلد معتقد است که بنزوات سدیم به تنهایی می تواند به اجزای حیاتی DNA در میتوکندری سلول آسیب برساند و آن ها را غیرفعال کند. میتوکندری در سلول در تولید انرژی نقش دارد و اگر آسیب ببیند سلول مختل شده و ممکن است واردآپوپتوزشود. بیماری های زیادی امروزه به آسیب DNAA نسبت داده می شود مانند پارکینسون و سایر بیمار ی های نابودی مغز و اعصاب (آلزایمر، هانتینگتون و ...)، و از همه مهتر، کلاً فرآیند پیری.[۸][۹][۱۰][۱۱][۱۲]
بیش فعالی
مقاله ای که در سال ۲۰۰۷م برای آژانس استاندارد غذایی (FSA) در انگلیس منتشر شد بیان کرد که برخی رنگ های مصنوعی هنگامی که بنزوات سدیم همراه شود می تواند با رفتار بیش فعالی در ارتباط باشد.[۱۳][۱۴][۱۵]
پروفسور جیم استیونسن از دانشگاه ساثمپتن و نویسنده ای این مقاله می گوید: <<این یک تحقیق عمده بوده است که روی موضوع مهمی انجام شده است. نتایج نشان می دهد که ترکیبات خاصی از رنگ های غذایی مصنوعی و نگهدارنده غذایی بنزوات سدیم با افزایش رفتار بیش فعالی در کودکان در ارتباط است. اما والدین نباید گمان کنند که با حذف این افزودنی ها از غذای کودکان از بروز اختلال بیش فعالی جلوگیری می شود. ما می دانیم که عوامل دیگری هم نقش دارند اما این حداقل چیزی است که کودک می تواند از آن اجتناب کند>>."[۱۵]
با بررسی های بیشتر توسط FSA چنین به نظر می رسید که فقط رنگ های خاصی در این مشکل نقش دارند.
در ۱۰ آوریل ۲۰۰۸ آژانس استاندارد غذایی خواستار حذف داوطلبانه ی رنگ ها (اما نه بنزوات سدیم) تا پایان سال ۲۰۰۹ میلادی شد.[۱۶]بعلاوه پیشنهاد کرد که اقدامی برای حذف تدریجی این مواد از غذاها و نوشیدنی ها در سطح اتحادیه ی اروپا در طی زمانی معین باید صورت گیرد.[۱۷]
در پاسخ به تأکید مصرف کنندگان بر محصولات طبیعی و ارتباط E۲۱۱ با تخریب DNA و ADHA (اختلال کم توجهی - بیش فعالی) شرکت کوکاکولا در حال حذف بنزوات سدیم از کوکای رژیمی است. این شرکت همچنین اعلام کرده است که قصد دارد E۲۱۱ را به محض این که جایگزین مناسبی برای آن یاف شود از سایر محصولات خود -- از جمله اسپرایت، فانتا و اویسیس -- نیز حذف کند.[۱۸]
نوشابه حاوی بنزوات سدیم ( ماده نگهدارنده ) است که بسیار سمی ، خطرناک و سرطان زاست .
بنزوات سدیم به شدت موجب آسیب سلول های کبدی می شود، کافئین و مواد رنگی در نوشابه برای قلب بسیار مضر بوده و سبب بی قراری و نامنظمی ضربان قلب می شود . کل نوشیدنی های صنعتی باعث پوسیدگی دندان ، چاقی ، سوء تغذیه ، سنگ کلیه ، چین و چروک در پوست ، پوکی استخوان بیماری های کلیوی و ... می شود .
شربت عسل با آبلیم تازه ، شربت عسل با عرق بهار نارنج ، شربت شاه توت ، و انواع دم کرده های گیاهی سالم ترین و پر خاصیت ترین نوشابه سنتی ایرانی به شمار می روند
| بنزوئیک اسید | |
|---|---|
 | |
| شناسنامه | |
| نام گذاری آیوپاک | Benzoic acid |
| جرم مولی | ۱۲۲٫۱۲ گرم بر مول |
| نما(ظاهر) | جامدسفید |
| دمای ذوب | ۱۲۲٫۴ درجه سانتی گراد |
| دمای جوش | ۲۴۹٫۲ درجه سانتی گراد |
| چگالی | ۱٫۲۶۵۹ گرم بر میلی لیتر (در ۱۵ درجهٔ سلسیوس) |
| فشار بخار | Not available |
| pH | ۳٫۰ محلول یک درصد |
| حلالیت در آب | کم محلول در آب سرد |
| چگالی نسبی بخار | ۴٫۲۱ (نسبت به هوا) |
بنزوئیک اسید، (C۷H۶O۲(C۶H۵COOH، یک ترکیببلوریبی رنگ (سفید دیده می شود) است. بنزوئیک اسید ساده ترینکربوکسیلیک اسیدآروماتیکنیز می باشد.
این ماده یکاسید ضعیفمحسوب می شود. از نمک های آن به عنوان نگهدارنده های غذایی استفاده می شود، همچنین در ساخت بسیاری از ترکیباتآلیدیگر از بنزوئیک اسید استفاده می شود.
| |
تاریخچه
بنزوئیک اسید در قرن شانزدهم میلادی کشف شد. اولین بار شخصی به نام Nostradamus از تقطیر خشک ماده ای سنتی به نام gum benzoin بدست آورد.
در سال ۱۸۷۵ شخصی به نام Salkowski نیز پی به خواص ضد قارچ بنزوئیک اسید برد.
تولیدکننده داخلی
تنها تولیدکننده اسیدبنزوئیک در ایران ،شرکت صنایع شیمیایی و سلولزی نگار آذربوده که در سه حالت پودر ، پرک و مایع محصولات خود را با بهترین کیفیت (خلوص بالای 99/999% طبق گواهی آزمایشگاه مرکزی دانشگاه تهران)به بازار عرضه می نماید و علاوه بر اسید بنزوئیک ، سدیم بنزوات نیز تولید می نماید . کارخانه: قم - شهرک صنعتی شکوهیه دفتر مرکزی: تهران - خیابان بهشتی - خیابان سرافراز - خیابان 10- پلاک 2 واحد 5 تلفن(6-88531645-021 و88734643و 88542028)فاکس 88548863 سامانه پیام کوتاه 300088542028
روشهای تهیه
روش تجاری
یکی از روشهای تجاری ساخت بنزوئیک اسید،اکسایشجزئیتولوئنبا گاز [
[اکسیژن]] در مجاورتکاتالیزورکبالتیامنگنز نفتناتاست که با بازدهٔ
بالا و رعایت اصول محیط زیستی (شیمی سبز) انجام می شود که تصویر واکنش مربوطه را در زیر می بینید: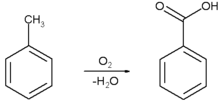
روش آزمایشگاهی
بنزوئیک اسید مادهٔ ارزان قیمت و در دسترسی است، در نتیجه در صورت نیاز به آن لازم نیست زحمت سنتز آن را متقبل شویم و فقط کافی است نمونهٔ تجاری آن را خریداری کرده و متناسب با کارمان آن را خالص سازی کنیم.
که برای اینکار استفاده از روشتبلور مجدد با دو حلالبا حلال هایاتانولو آب بسیار مناسب می باشد.
ولی در هر صورت می توان آن را به روش های زیر نیز سنتز کرد:
باهیدرولیز
ازهیدرولیزبنزونیتریل،بنزآمیددر محیط هایاسیدیو یابازیشدید می توان بنزوئیک اسید یاآنیونآن را بدست آورد
ازبنزالدهید
همچنین می توان با استفاده از واکنشکانیزارو ی تقاطعیبنزوئیک اسید را ازبنزالدهیدساخت که واکنش مربوط به آن را در زیر می بینید:
از بنزیل الکل
همچنین می توان ازاکسایشبنزیل الکلدر حضور محلولپتاسیم پرمنگناتداغ نیز استفاده کرد.
در این روش بلافاصله بعد از واکنش باید محلول در حالت داغ فیلتر شود تامنگنز دی اکسیدتشکیل شده جدا شود و سپس محلول به حال خود رها می شود تابلورهایبنزوئیک اسید تشکیل شود.
مصارف
به عنوان خوراک واحدهای صنعتی
برای تهیهٔ بنزیل کلرید
بنزیل کلرید(C۶H۵COCl) از واکنشتیونیل کلرید(یاپنتاکلرید فسفریاتری کلرید فسفریافسژن) با بنزوئیک اسید به دست می آید. با استفاده ازبنزیل کلریدمی توان بسیاری ازمشتقاتبنزوئیک اسید را ساخت از جملهبنزیل بنزوآتکه یک طعم دهندهٔ مصنوعی می باشد.
برای تهیهٔفنول
فنول(C۶H۵OH) ازکربوکسیل زداییهمراه بااکسایشدر دمای ۳۰۰oC الی ۴۰۰oC بدست می آید. البته این فرایند می تواند در حضورکاتالیزورنمککبالتII در ۲۰۰oC هم انجام پذیرد.فنول(Phenoll) نیز استفاده های بسیاری دارد، که مهمترین آنها تبدیلفنولبهسیکلوهگزانولمی باشد که سرآغازی برای تولیدنایلوناست.
وبرای ساخت بسیاری مواد دیگر
نگهدارندهٔ غذا
بنزوئیک اسید و نمک هایش به عنوان نگهدارندهٔ غذا مصرف دارند که به نام های E۲۱۲، E۲۱۱، E۲۱۰ و E۲۱۳ شناخته می شوند. هر کدام از این نمک ها از واکنش مستقیم یا واکنش با نمک هایسدیم،پتاسیمیاکلسیمتهیه می شوند.
در اصل بنزوئیک اسید از رشدقارچها،مخمرهاو بعضیباکتریهاجلوگیری می کند. نحوهٔ اثر بنزوئیک اسید اینگونه است که در ابتدا بنزوئیک اسید جذبسلولمی شود، اگرpHدرونسلولیبه ۵۵ یا کمتر تغییر کند،تخمیر ناهوازیگلوکزاز طریق Phosphofructokinase به میزان ۹۵۵٪ کاهش می یابد و این خود باعث نابودی آنها می شود. مقدار معمول استفاده از بنزوئیک اسید و نمک هایش به عنوان نگه دارنده بین ٪۰٫۰۵-٪٪۰٫۱ می باشد. البته در بعضی غذاها باید از سطوح بالاتری از بنزوئیک اسید استفاده شود که مقادیر ماکسیمم آن در قوانین بین المللی غذا موجود است.[۱][۲]
البته نگرانی هایی وجود دارد مبنی بر اینکه بنزوئیک اسید باآسکوربیک اسید(ویتامین C) موجود درنوشابه هاواکنش داده و مقادیر بسیار کم (ولی در دراز مدت خطرناک)بنزنتولید می شود.[۳]
دارو
اسید بنزوئیک جزئی از پماد Whitfield است که برای درمان بیماری هایقارچیپوستومواستفاده می شود.[۴][۵]
خطرات بنزوئیک اسید
بنزوئیک اسید یک محرک پوست و چشم است. پس باید از تماس آن با پوست و چشم احتراز شود
برچسب : نویسنده : csina956 بازدید : 226
آرشیو مطالب
لینک دوستان
- کرم سفید کننده وا
- دانلود آهنگ جدید
- خرید گوشی
- فرش کاشان
- بازار اجتماعی رایج
- خرید لایسنس نود 32
- خرید بانه
- خرید بک لینک
- کلاه کاسکت
- موزیک باران
- دانلود آهنگ جدید
- ازن ژنراتور
- نمایندگی شیائومی مشهد
- مشاوره حقوقی تلفنی با وکیل
- کرم سفید کننده واژن
- اگهی استخدام کارپ
- هاست ایمیل
- دانلود فیلم
- آرشیو مطالب
- فرش مسجد
- دعا
- لیزر موهای زائد
- هاست ایمیل
- رنگ مو
- شارژ
